5.食事性酸塩基負荷のメカニズム
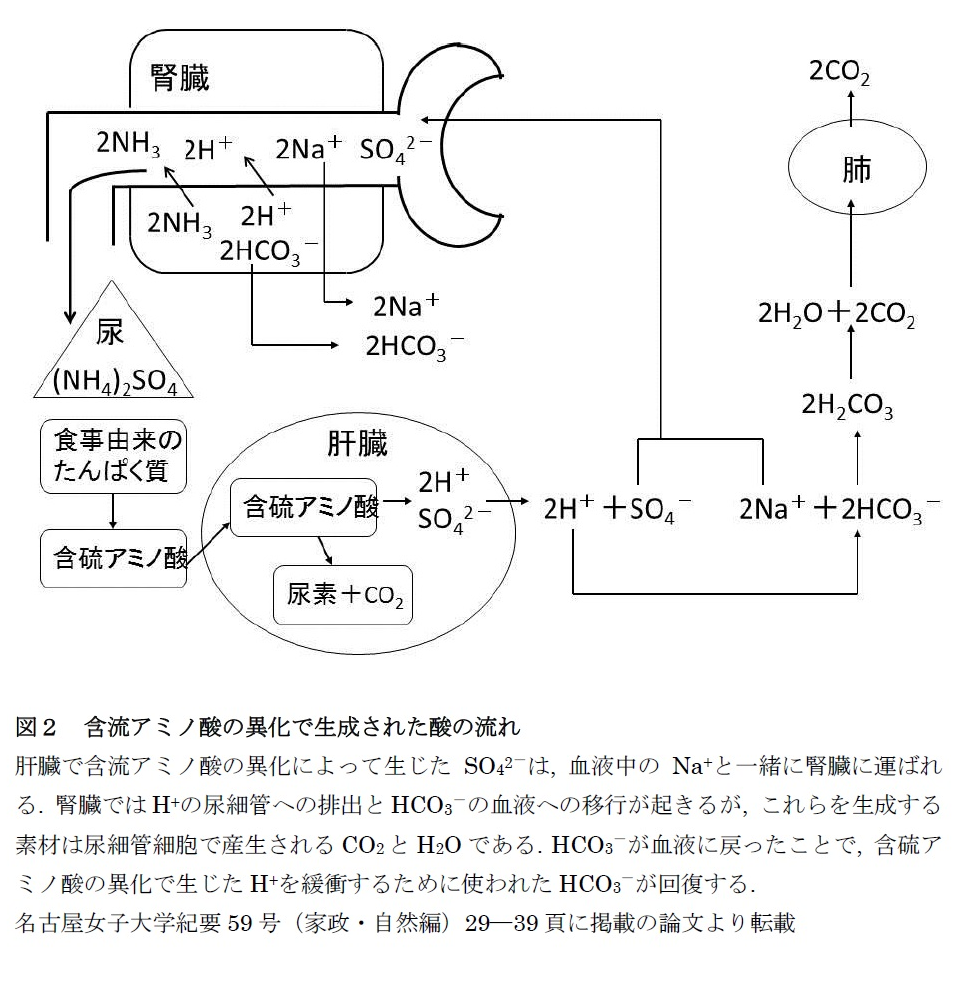
代謝による酸塩基の生成 ――― 肝臓や他の臓器で行われる代謝の過程で酸または塩基の産生が起きます。一例として、肝臓で含流アミノ酸が代謝される様子を見てみましょう(図2)。一般的なアミノ酸の異化代謝によって作られる尿素は中性ですが、含硫アミノ酸に含まれるSが代謝されるとSO42-と2 H+が生成します。 生じたH+と血液中のHCO3-とからH2CO3が作られ、肺からCO2として呼気中に排泄されます。 一方、SO42-は血液中の2 Na+と一緒に腎臓に運ばれると、 Na+はNa+‐H+交換輸送体を介して尿細管から再吸収されて血中に戻ります。これと同時に尿細管腔へH+が排出されます。 このH+は、尿細管上皮細胞でCO2とH2Oから新しく作られたものです。同時に生成するHCO3-は血中へ入ります。腎臓はpH 4.4より酸性の尿を生成することができないので、H+は集合管へ排泄されるNH3と結合し、NH4+となって尿中へ排出されます。なお、血中に戻ったHCO3-は、Sの代謝で生じたH+を受け取るのに使われたHCO3-を補充します。
また、 野菜や果実に含まれる有機酸のアルカリ塩は体内に取り込まれると、有機酸は異化反応でCO2とH2Oになって、最終的にHCO3-のアルカリ塩を生じるので塩基が増えることになります。 クエン酸ナトリウム(Na3C6H5O7)を例にして説明しましょう。 先ず, 肝臓などの臓器のミトコンドリアにおいて次の反応が進みます。
2Na3C6H5O7 + 6H+ + 9O2 → 12CO2 + 8H2O + 6Na+
生成したCO2は血中でH2Oと反応してH2CO3となります。H2CO3が解離してできたHCO3-がクエン酸ナトリウム由来のNa+と対になって血液中に保持されます。このことは上の反応式を変形して次のように表せます。
このように血液中のNaHCO3が増えるので塩基負荷が生じます。 NaHCO3が過剰なときは腎臓から尿へ排出されます。
2Na3C6H5O7 + 9O2 → 6CO2 + 2H2O + 6HCO3-+ 6Na+
このように血液中のNaHCO3が増えるので塩基負荷が生じます。 NaHCO3が過剰なときは腎臓から尿へ排出されます。
イオンの腸管吸収率の違いによる酸負荷 ――― Remerは、陰イオンと陽イオンの腸管吸収率の違いによって酸負荷を生み出す様子を、CaCl2の場合について次のように説明しています(図3)。腸管吸収率が25%であるCaは約1/4の量が腸管から血液内に吸収され、吸収率が95%であるClはほとんど全部が吸収されます。その結果、血中にCa2+より過剰のCl-が入ることになります。 そして、過剰分のCl-と陰陽イオンのバランスが取れるように 膵臓から分泌されたNaHCO3由来のNa+が吸収されて血中に入ります。腸管に残ったHCO3-は、吸収されなかった3/4のCa2+と塩を形成して便に排泄されるので、血液のHCO3-が減少します。 このように、 血液におけるHCO3-の不足、即ち酸負荷が起きます。 実際に、CaCl2を摂取したときNAEが増加するとともに尿pHが低下することが観察されています。
「酸性食品・アルカリ性食品」の一般的な議論で、リンたんぱく質を摂取した場合に、酸負荷が起こるとされています。 Remerも、文献1の中でリンたんぱく質が腸管で加水分解されるとアミノ酸とリン酸(2H++HPO42-)を生成することを説明しています。しかし、リン酸エステルのpKa(一般的な糖のリン酸エステルの値から推測して6付近)から判断すると、 小腸内のpHではリン酸エステルの加水分解によってほとんどH+が遊離されないので、リンたんぱく質の腸管吸収は、次のように考えるべきであろうと思います。
リンたんぱく質は小腸で消化を受けるとO‐ホスホセリンやO‐ホスホスレオニンが生じ、さらにアミノ酸とリン酸に加水分解されます。リンたんぱく質がマグネシウム塩あるいはカルシウム塩として摂取されるとすると、CaやMgの吸収率がリン酸塩より低いので、 CaCl2の場合と同様に酸負荷が生じます。しかし、リンたんぱく質がナトリウム塩かカリウム塩の場合は、NaやKの吸収率がリン酸塩より高いため、逆に塩基負荷が生じます。このようなことから、リン含量の多い食事の摂取によって単純に酸負荷が生じるとは限りません。リン酸のアルカリ塩の腸管吸収についても同じことが言えます。
血中に入ったHPO42-は、2個のNa+と一緒に腎臓に運ばれると、比較的再吸収されにくいので 尿細管内液に留まりますが、 Na+は 尿細管からNa+‐H+交換輸送体によって再吸収されます。このとき同時にH+が 尿細管腔へ排出されます。そして、HPO42-がこのH+を受け取ってH2PO4-となり、Na+を伴って尿に排出されます。H+の起源は、尿細管上皮細胞におけるCO2とH2Oとの反応です。この反応で同時に生成するHCO3-が血中へ入ります。リン酸塩の腸管吸収で酸負荷が生じるときには、このように尿にHPO42-が排泄されるときに、H+の排出が伴います。
PRALを応用した研究例 ――― PRALや推定NAEがこれまでに多数の研究において利用され, 食物中ミネラル量と尿中酸排泄量とを関連づける証拠が蓄積されてきました。 それらの研究例を見てみましょう。 まず、参考にした文献を掲げておきます。
6) Michaud, D. S., Troiano, R. P., Subar, A.
F., Runswick, S., Bingham, S., Kipnis, V., and Schatzkin, A. : Comparison of
estimated renal net acid excretion from dietary intake and body size with urine
pH, J. Am. Diet. Assoc., 103, 1001-1007 (2003)
7)Welch, A. A., Mulligan, A., Bingham, S. A.,
and Khaw, K. T. : Urine pH is an indicator of dietary acid-base load, fruit and
vegetables and meat intakes: results from the European Prospective
Investigation into Cancer and Nutrition (EPIC)-Norfolk population study, Br. J.
Nutr., 99, 1335-1343 (2008)
8) Ausman, L. M., Oliver, L. M., Goldin, B.
R., Woods, M. N., Gorbach, S. L., and Dwyer, J. T. : Estimated net acid
excretion inversely correlates with urine pH in vegans, lacto-ovo vegetarians,
and omnivores, J. Ren. Nutr., 18, 456-65 (2008)
9) Fenton, T. R., Lyon, A. W., Eliasziw, M.,
Tough, S. C., and Hanley, D. A. : Meta-analysis of the effect of the acid-ash
hypothesis of osteoporosis on calcium balance, J. Bone Miner. Res., 24,
1835-1840 (2009)
10)Cao, J. J., Johnson, L. K., and Hunt, J. R. :
A diet high in meat protein and potential renal acid load increases fractional
calcium absorption and urinary calcium excretion without affecting markers of
bone resorption or formation in postmenopausal women, J. Nutr., 141,
391-397 (2011)
11)Breslau, N. A., Brinkley, L., Hill K. D.,
Pak, C. Y. : Relationship of animal protein-rich diet to kidney stone formation
and calcium metabolism, J. Clin. Endocrinol. Metab., 66, 140-146
(1988)
12) Murakami, K., Sasaki, S., Takahashi, Y.,
Uenishi, K., and Japan Dietetic Students' Study for Nutrition and Biomarkers
Group: Association between dietary acid-base load and cardiometabolic risk
factors in young Japanese women, Brit. J. Nutr., 100, 642-651
(2008)
自由生活をしている人を対象にして、食事内容とNAEないし尿pHとの関係を調べた疫学研究がいくつか発表されています.
・ Michaudら(文献6)は, 米国メリーランド州モンゴメリー郡で次のような疫学研究(男女484人, 平均年齢53歳)を行い、食品摂取頻度調査および24時間思い出し法による食事調査からの推定NEAが24時間尿のpHと逆相関することを示しました。
・Welchら(文献7)は, 英国ノルフォークの39~78歳の住民22,038人を対象にしてPRALおよび摂取食品群(果実・野菜, 肉, 穀類, 乳製品)と尿pHとの関係を調べるとともに, サブグループ363人に対して1回尿および24時間尿のpH測定と7日間の食事調査を行い, 果実・野菜が多く肉が少ない食事ほど, 尿pHが高くなることを示しました。
・Ausmanら(文献8)が米国ボストンの女性で完全菜食主義者(10人), 乳・卵を摂る菜食主義者(16人)および雑食の人(16人)の尿pHを調べた結果(平均値 + SD)は, それぞれ6.15 + 4.10, 5.90 + 0.36, 5.74 + 0.12でした。 また, 各群6人のサブグループにつき3日間の食事調査から得た推定NAEは, 17.3 + 14, 31.3 + 8.5, 42.6 + 3.2 mEq/日で, 尿pHと推定NAEの間に有意な負の相関が認められました。
・ Michaudら(文献6)は, 米国メリーランド州モンゴメリー郡で次のような疫学研究(男女484人, 平均年齢53歳)を行い、食品摂取頻度調査および24時間思い出し法による食事調査からの推定NEAが24時間尿のpHと逆相関することを示しました。
・Welchら(文献7)は, 英国ノルフォークの39~78歳の住民22,038人を対象にしてPRALおよび摂取食品群(果実・野菜, 肉, 穀類, 乳製品)と尿pHとの関係を調べるとともに, サブグループ363人に対して1回尿および24時間尿のpH測定と7日間の食事調査を行い, 果実・野菜が多く肉が少ない食事ほど, 尿pHが高くなることを示しました。
・Ausmanら(文献8)が米国ボストンの女性で完全菜食主義者(10人), 乳・卵を摂る菜食主義者(16人)および雑食の人(16人)の尿pHを調べた結果(平均値 + SD)は, それぞれ6.15 + 4.10, 5.90 + 0.36, 5.74 + 0.12でした。 また, 各群6人のサブグループにつき3日間の食事調査から得た推定NAEは, 17.3 + 14, 31.3 + 8.5, 42.6 + 3.2 mEq/日で, 尿pHと推定NAEの間に有意な負の相関が認められました。
次に、尿pHないしNAEと関係した疾病予防の話題を二三取り上げます。尿中酸排泄と骨代謝への悪影響との関連については論議があります。高たんぱく質食を摂取すると、その代謝で生じる酸を中和するために骨からCaが遊離するという主張があります。しかし, 最近のメタアナリシスの結果はこの主張に否定的です。 NAEと1日の尿Ca排泄量との間で有意な相関が認められるが, NAEの変化はカルシウムバランス(摂取量 - 尿と便への排泄量)の変化と相関しなかったと言うことです。しかも骨代謝マーカーの変化とも相関しなかったので, NAEが高くCa排泄量が多くても、全身からのCaの損失は起きていないことになります(文献9)。 このことと関連した別の研究では, 閉経後の女性16人を対象に, 食肉摂取(高PRALの食事)と低たんぱく質食(低PRALの食事)を7週間ずつ供給する無作為クロスオーバー研究を行い, 尿中Ca排泄の増加が腸管からのCaの吸収の増加によることを観側しています(文献10)。 高たんぱく食によって尿へのSO42-の排出が多いときは, 腸管からのCa2+吸収を増やして尿中Ca2+量を高めてSO42-とのバランスを取ろうとする生理的機構が働いているようです。
食事と尿酸結石との関係の話題に移ります。高動物たんぱく質食で尿への尿酸排泄が高まることは、よく知られています。同時に、尿が酸性に傾くので尿酸が非解離型になるため尿酸の溶解度が低下します。 菜食主義者と高動物タンパク質食の人の尿の非解離型尿酸の濃度を比較すると, 高動物タンパク質食の人で有意に高いことが報告されています(文献11)。 痛風患者の結石予防のため, アルカリ製剤の投与が行われることがありますが, そのようなときには当然尿が酸性に偏らいような食事が好ましいことになります。
我が国からもPRALを用いた研究の報告があります。PRALと代謝危険因子の関連を18~22歳の女子学生1,136人を対象に調査して, PRALの値が高いほど血圧, 総コレステロール, LDL‐コレステロールが高いことが報告されています(文献12)。 即ち, 食事性酸負荷の低い食事は生活習慣病の予防に適していることになります。 動物性食品と植物性食品のバランスがよい食事はPRALの値が高くなるので、食事性酸負荷が低いこと自体が原因であるかどうかは不明です。
6.おわりに
このようにPRALを用いた論文が国際誌に多数発表されていることから, 食事性酸負荷の概念が世界の栄養学関係者に認知されていることが分かります。 さらに, 2007年のThe Journal of NutritionのIssues
and Opinionsとして, 推定NAEの計算に用いるアルゴリズムや用語を研究者間で確認した記事が出ています。このような状況を鑑みると, 食事性の酸塩基負荷に関する知識は、栄養学の教育において無視できないと考えられます。そして、これまで異端視されてきた「酸性食品」・「アルカリ性食品」を従来のイメージを払拭して「酸負荷食品」・「塩基負荷食品」と名称を変えるなどして栄養学の中で復活させるべきであると思います。
これで「酸性食品・アルカリ性食品」再考のお話は終わりです。重炭酸塩(HCO3-)を塩基、炭酸(H2CO3)を酸ととらえて説明してきましたが、酸塩基平衡の詳細に立ち入りませんでした。次回は、管理栄養師養成校でよく質問を受けた血液の酸塩基平衡の生理学について説明をします。
無断転載禁止

0 件のコメント:
コメントを投稿